О чем эта статья
Обзор
Институт медицины определил пищевые антиоксиданты в соответствии с их способностью смягчать негативное воздействие активных форм оксидантов на нормальные физиологические функции человека. Хотя польза пищевых антиоксидантов для здоровья общепризнана, они все же не могут предотвратить или защитить человека от хронических заболеваний благодаря своему антиоксидантному действию. Несмотря на то, что наиболее важным конечным результатом использования антиоксидантов в диете является снижение риска изучаемых нами заболеваний у людей, для установления истинного механизма их действия необходимо провести комплексное тестирование и оценить состояние окислительного стресса, которое будет отражать как само действие, так и эффективность применения пищевых антиоксидантов. В этом контексте в данной статье обсуждается клиническое значение пищевых антиоксидантов при метаболическом синдроме.
Введение
Реактивные окислители, включая активные формы кислорода (ROS), активные формы азота (RNS) и активные формы серы (RCC), представляют собой электрофилы, которые отбирают один или два электрона у нуклеофила без образования аддукта. (1) Они производятся как часть нормальной физиологии человеческого организма, однако считается, что их неконтролируемое производство может привести к возникновению и развитию ряда заболеваний, таких как рак, ожирение, сахарный диабет, метаболический синдром, сердечно-сосудистые заболевания (ССЗ), неврологические расстройства, гипертония и катаракта. (2)
Развитие и прогрессирование этих заболеваний наблюдается, в частности, в условиях, когда выработка реактивных оксидантов подавляет потенциал системы антиоксидантной защиты организма и возникает окислительный стресс. (3) Увеличение потребления антиоксидантов с пищей считается одним из простейших способов укрепить защитные силы организма. Пищевые антиоксиданты, которые включают в себя основные питательные антиоксиданты, такие как витамины C и E и ряд минералов (кофакторы антиоксидантных ферментов), а также менее важные фитохимические вещества, обычно встречаются во многих растительных продуктах и лекарственных растениях, и их роль в профилактике и лечении хронических заболеваний, связанных с действием реактивных оксидантов. (4-6)
Например, потребление нескольких антиоксидантов в рационе считается профилактическим или даже терапевтическим средством против заболеваний реактивной окислительной этиологии. Однако данные наблюдений и клинические данные о влиянии пищевых антиоксидантов в лучшем случае противоречат друг другу. Некоторые исследования даже показали, что прием дополнительных антиоксидантов может увеличить риск смерти при определенных условиях. (7-9)
Антиоксиданты могут снизить риск сердечно-сосудистых заболеваний и диабета благодаря своей способности поглощать реактивные типы оксидантов. Однако не менее важно признать, что они могут улучшить здоровье человека с помощью других своих механизмов. (5, 10) Наличие некоторых взаимосвязей между некоторыми типами оксидантов и активными антиоксидантами позволило нам предположить, что окислительный стресс каким-то образом связан с явлениями, которые происходят на ранних стадиях развития метаболического синдрома (МетС), такими как и с последствиями этих явлений. Например, динамическое взаимодействие между окислительным стрессом и комбинацией факторов риска развития метаболического синдрома, включая дислипидемию, гипергликемию, гипертензию и ожирение, может привести к диабету 2 типа и сердечно-сосудистым заболеваниям. (11) Последовательное исследование антиоксидантной защиты и биологических маркеров окислительного стресса во время развития метаболического синдрома обеспечивает надежный подход для проверки гипотетической гипотезы, приведенной выше, и установления истинной пользы пищевых антиоксидантов для здоровья человека.
В этом кратком обзоре мы рассматриваем данные исследований на людях, направленные на установление точной роли антиоксидантов и активных оксидантов в возникновении и прогрессировании метаболического синдрома, а также в вероятном риске последующего развития диабета и сердечно-сосудистых заболеваний.
Основные патологические процессы, инициируемые чрезмерной активацией ПОЛ:
I. УРОВЕНЬ КЛЕТОЧНОЙ ТКАНИ:
1. Ишемия;
2. Гипоксия;
3. Мембранопатия:
- чрезмерное скопление свободных радикалов внутри клетки;
- накопление ионов Са ++ внутри клетки++;
- нарушение проницаемости клеточной мембраны и мембран клеточных органелл
- выброс лизосомальных ферментов в клетку;
4. Апаптоз и некроз клеток;
5. Нарушение связи с мобильным телефоном;
6. Энергетические и метаболические расстройства.
II. ОРГАНЫ И СИСТЕМЫ:
1. Функциональные расстройства;
2. Органическая патология.

Рис. 3. Окислительный стресс при гипоксии
Конечно, в организме есть эндогенная антиоксидантная система, но при критических уровнях гипоксии и перекисного окисления липидов она неустойчива. Антиоксидантная система организма (АОС) состоит из водорастворимых и жирорастворимых ферментов и субстратов. Основным механизмом антиоксидантной защиты in vivo является фермент супероксиддисмутаза (СОД), окисление которого позволяет инактивировать свободные радикалы в месте образования, предотвращая их диффузию.
Большинство клеток могут переносить умеренную степень окислительного стресса из-за того, что у них есть восстановительная система, которая идентифицирует и удаляет окислительно поврежденные молекулы, которые затем заменяются. Кроме того, клетки могут повышать свою антиоксидантную защиту в ответ на окислительный стресс. Однако в условиях сильного окислительного стресса все молекулы живых организмов (липиды, белки, нуклеиновые кислоты и углеводы) могут быть потенциальными целями окислительного повреждения.
Поскольку формирование тканевой гипоксии, ПОЛ, митохондриальной дисфункции признано стартовым звеном в развитии типичного патологического процесса, применение антигипоксантов и антиоксидантов патогенетически оправдано при любой острой патологии.
Термин «антиоксиданты» появился в 60-х годах ХХ века благодаря исследованиям Б. Н. Тарусова (1954), Н. М. Эмануэля (1963). Б. Н. Тарусов установил роль липидов, в частности ненасыщенных жирных кислот, как одного из основных субстратов биохимических процессов, оценил радиозащитное действие цистеина, глутатиона и тиомочевины. Н. М. Эмануэль и его ученики не только определили механизм действия антиоксидантов, но также определили антиоксиданты как соединения, которые подавляют развитие свободнорадикального окисления.
Антиоксидантные препараты — это препараты различной химической структуры, которые подавляют или блокируют процессы окисления свободных радикалов и / или способствуют повышению уровня веществ с антиоксидантным действием в организме (рис. 4).
По своим химическим свойствам антиоксиданты (АО) делятся на 2 группы: «ловушки радикалов», которые напрямую взаимодействуют со свободными радикалами, и «поглотители» (детергенты), разлагающие продукты радикального окисления (FRO) с их последующей инактивацией и использовать.

Рис. 4. Механизм действия антиоксидантов
Разработаны и изучаются многочисленные препараты с антигипоксантно-антиоксидантными свойствами (Мексидол, Цитофлавин, Танакан, Актовегин, Кортексин, Цитофлавин, ПК-Мерц, Аминалон, Цераксон, Эспалипон, Церебро и др.). Многие из них уже доказали свою высокую эффективность у пациентов в отделении интенсивной терапии, особенно в нейрокритическом отделении (это отдельная тема). Однако с научной точки зрения ОС, ее значение в критическом состоянии и антиоксидантной коррекции (ОИМ, травмы головы, кровопотеря, хирургическое вмешательство, анестезия и т.д.) изучены очень мало. А в практическом применении мониторинг степени ОС и эффективности ее коррекции антиоксидантами в больницах вообще не проводится.
Причины такой ситуации, прежде всего, в незнании врачей ОС. Читая уроки на курсах повышения квалификации, мы убедились, что анестезиологи-реаниматологи не очень ориентируются в этой проблеме. Стоит вспомнить слова В.И. Вернадского: «Нет неизлечимых болезней, есть недостаток знаний». Использование антиоксидантов в практическом здравоохранении ограничивается полным отсутствием в лабораториях и больничных палатах оборудования, которое измеряет и отслеживает изменения в AOS и OS пациентов, за исключением этих препаратов в «стандартах» лечения (например, за исключением лечения инсультов.). Между тем эмпирическая медицина уже опередила научные разработки и «стандарты» в лечении критических состояний. Таким образом, в Красноярской краевой больнице уже накоплен многолетний положительный опыт применения антиоксидантов-антиоксидантов при лечении тяжелых ожогов и черепно-мозговой травмы, гнойно-септических состояний, операций на головном мозге и сердце, комы различной этиологии.
На примере одного препарата Мексидол из большой группы антиоксидантов можно понять, насколько полезны и необходимы эти препараты в интенсивной терапии критических состояний.
Мексидол — это международное название сукцината оксиметилэтилперидина. Обладает высокой биодоступностью и липофильностью. Он быстро переходит из кровотока в органы и ткани и быстро выводится из организма. Благодаря наличию в своем составе производного 3-гидроксипиридина, которое является активным вектором, он проникает в клетку и митохондрии (Думаев К.Н., 1995). Препарат практически не токсичен.
Рис. 5. Характеристики реакции цикла Кребса, связанной с сукцинатом
1. Окисление сукцината является предпосылкой для каталитического действия промежуточного продукта на ассимиляцию кислорода клеткой.
2. Чтобы восстановить пул органической кислоты, просто добавьте сукцинат.
3. Активность сукцинатдегидрогеназы не зависит от концентрации НАД и НАДхН.
4. Мощность системы генерации на ЯК в сотни раз выше, чем у всех остальных систем.
5. Явление быстрого окисления сукцината в цитоплазме клеток с восстановлением динуклеотидов.
Производные 3-гидроксипиридинов (в составе Мексидола):
- Они играют важную роль в обмене веществ.
- Необходим для нормального функционирования центральной нервной системы.
- Они входят в состав ферментов, осуществляющих декарбоксилирование и периаминирование аминокислот.
- Участвует в обмене триптофана, метионина, цистеина, гистамина, глутаминовой и других аминокислот.
- Участвует в процессах липидного обмена.
Экспериментальные и клинические исследования продемонстрировали эффективность использования антиоксидантов при лечении ОИМ и инсульта. При ишемии миокарда происходит ограничение зоны некроза в миокарде (рис. 6); повышенная биоэлектрическая активность сердца; улучшение гемодинамики и переносимости сердечного стресса.

Рис. 6. Ограничение зоны некроза миокарда Мексидолом

Рис. 7. Влияние антиоксидантов на продолжительность жизни
Таблица 1
Причины и признаки дефицита
При недостаточном поступлении в организм антиоксидантов люди теряют ясность мысли, снижается трудоспособность, слабеет иммунитет, ухудшается зрение, развиваются хронические заболевания. Антиоксиданты ускоряют процесс заживления, помогают продлить жизнь и уменьшить повреждение тканей.
Рассмотрим причины истощения запасов каротиноидов, минералов, витаминов в организме человека и то, что улучшает образование свободных радикалов:
- Воздействие тепла.
- Усталость.
- Загрязнение атмосферы, воды, ядохимикатов, бытовой химии.
- Табачный дым.
- Ультрафиолетовые лучи солнца, радиация.
- Раны и раны.
- Чрезмерная физическая нагрузка.
- Заражение паразитами, вирусами, бактериями.
- Недостаток в рационе натуральных антиоксидантов.
- Гипоксия.
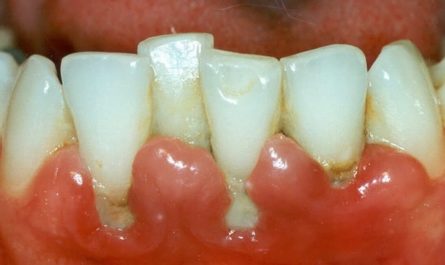
Симптомы дефицита антиоксидантов в организме:
- кровоточащие десны;
- потеря зубов, волос;
- быстрая утомляемость;
- появление преждевременных морщин, высыпаний;
- повышенная раздражительность, нервозность;
- частые инфекционные заболевания;
- мышечная слабость;
- низкая эффективность;
- апатия;
- мурашки по коже на локтях;
- снижение остроты зрения, половой функции;
- плохой сон;
- депрессия;
- замедление роста.
- сухая кожа;
При индивидуальной непереносимости витаминов и минералов — антиоксидантов потребность в соединениях снижается.
Роль витаминных антиоксидантов
Самыми крупными поглотителями свободных радикалов в организме являются витамины C, E, A.
Эти антиоксиданты можно получить с пищей, однако из-за сильно загрязненной окружающей среды потребность человека в этих веществах увеличивается с каждым годом, в результате становится все труднее восполнить дефицит с помощью природных источников. В этом случае на помощь приходят витаминизированные добавки, которые благотворно влияют на работу внутренних органов, улучшают общее самочувствие человека.
Роль антиоксидантов:
- Витамин Е (токоферол). Он внедряется в клеточные мембраны, отражает атаку свободных радикалов, предотвращает разрушение, повреждение тканей. Кроме того, витамин E замедляет перекисное окисление и стабилизирует внутриклеточные процессы. Токоферол блокирует преждевременное старение кожи, предотвращает развитие катаракты, укрепляет иммунную систему, улучшает всасывание кислорода.
- Витамин А (ретинол). Этот антиоксидант частично синтезируется из бета-каротина, который, в свою очередь, ослабляет воздействие химического и радиоактивного загрязнения, электромагнитного излучения и повышает сопротивляемость организма стрессу. Витамин А защищает слизистые оболочки внутренних органов, кожу от вредных факторов окружающей среды, помогает иммунной системе нейтрализовать бактерии и вирусы. Он уничтожает канцерогены, вызывающие рост злокачественных опухолей, снижает уровень холестерина, предотвращает сердечные заболевания и инсульт. При хроническом недостатке ретинола увеличивается активность свободных радикалов, отмечается сухость кожи, ухудшается зрение.
- Витамин С (аскорбиновая кислота). Он защищает клетки мозга и другие антиоксиданты (токоферол) от свободных радикалов. Витамин С увеличивает синтез интерферона, нейтрализует токсины и стимулирует работу нервных клеток. Интересно, что одна выкуренная сигарета разрушает 100 миллиграммов аскорбиновой кислоты.
Помните, что сами по себе витамины обладают недостаточной антиоксидантной активностью и без комбинированного действия минералов они не могут полностью защитить организм от вредных факторов (эндогенных и экзогенных).
Активные виды окислителей и антиоксиданты
Реактивные окислители — это атомы, молекулы или ионы с неспаренными электронами, которые чрезвычайно нестабильны и обладают высокой реакционной способностью. Предпочитая принимать дополнительный электрон от других нестабильных молекул, они также могут отдавать свой электрон другим молекулам. (12) Их можно получить из трех элементов: кислорода, азота и серы. Следовательно, различают активные формы кислорода, активные формы азота и активные формы серы. Организм человека обычно содержит АФК в виде супероксид-аниона (O2–), гидропероксильного радикала (HO2), гидроксильного радикала (OH), оксида азота (NO), пероксида водорода (H2O2), синглетного кислорода (1O2), хлорной кислоты (HOCl), пероксинитрит (ONOO-). (6) Реактивные оксиданты постоянно вырабатываются в организме как ферментативными, так и неферментативными механизмами. (1, 3) Ферментные механизмы включают индукцию ксантиноксидазы во время гипоксии, респираторный взрыв иммунных клеток в ответ на инфекции и синтез простагландинов. Неферментативные механизмы включают образование супероксидов в митохондриях, когда электроны покидают цепь переноса электронов во время производства АТФ, а также образование гидроксильных радикалов из H2O2 во время реакции Фентона, где ионы железа действуют как медиаторы. Их образование становится более активным, если человеческий организм подвергается воздействию рентгеновских лучей, озона, табачного дыма и загрязненного воздуха. (1, 3) Было подсчитано, что от 1 до 3% кислорода, которым мы дышим, становится реактивным окислителем, и это число может увеличиваться во время упражнений.
Чтобы защитить себя от постоянного воздействия активных форм оксидантов, человеческий организм оснащен достаточно эффективной системой антиоксидантной защиты. Однако некоторые активные типы окислителей все еще способны обходить защитную систему и атаковать близлежащие чувствительные молекулы. Система антиоксидантной защиты бывает двух типов: эндогенная и экзогенная. Эндогенную защитную систему можно разделить на три подвида:
- защита антиоксидантными ферментами (супероксиддисмутаза, глутатионпероксидаза, каталаза, тиоредоксинредуктаза, хинонредуктаза);
- белковая защита (ферритин, трансферрин, церулоплазмин);
- защита с помощью низкомолекулярных антиоксидантов (глутатион, тиоредоксин, липоевая кислота, убихинол, мочевая кислота).
Эндогенная система защиты организма может быть усилена такими стимулами, как энергичные упражнения и диетические полифенолы. Экзогенная система защиты состоит из витаминов С и Е, каротиноидов, фенольных кислот, флавоноидов и других веществ, которые попадают в организм человека исключительно с пищей: фрукты, овощи, цельнозерновые и орехи. Увеличение потребления антиоксидантов с пищей обычно эффективно для повышения антиоксидантной защиты. Есть несколько определений пищевых антиоксидантов. Институт медицины определил пищевой антиоксидант как «вещество, присутствующее в пище, которое значительно снижает негативное влияние активных форм кислорода, активных форм азота или того и другого на нормальную физиологическую функцию человека». Это определение было основано на следующих трех критериях: 1) присутствие вещества в рационе человека, 2) наличие измерений содержания вещества в пищевых продуктах, обычно потребляемых людьми, 3) доказательства того, что вещество снижает вредное воздействие активных форм кислорода и азота на теле человека in vivo. (13) Несколько иное определение было дано Хлебниковым и его коллегами (14), которые определили антиоксидант как «любое вещество, которое непосредственно абсорбирует химически активные формы окислителей или оказывает косвенное действие, приводящее к усилению антиоксидантной защиты или« ингибированию производства » активных окисляющих веществ ». С нашей точки зрения, именно это определение включает те вещества, которые, обладая слабой способностью абсорбировать радикалы, все же способны увеличивать общую антиоксидантную способность организма за счет индукции системы эндогенной антиоксидантной защиты.
Употребление растительной пищи обратно связано с риском многих заболеваний. Вероятно, это связано с высокой плотностью питательных веществ и фитохимических веществ в растительной пище. Для людей, ведущих здоровый образ жизни и потребляющих здоровую пищу для предотвращения возможных заболеваний, витамины C и E наиболее известны своей антиоксидантной активностью всех основных питательных микроэлементов. Витамин C эффективен при удалении O2, 1O2, OH и RNS из организма. (15) Витамин E действует как мощный липофильный антиоксидант, который останавливает распространение перекисного окисления липидов, отдавая свой фенольный водород пероксильным радикалам, которые образуют токофероксильные радикалы, которые, хотя они также являются радикалами, неактивны для продолжения реакции окислительной цепи. Подобно витамину Е, но даже более эффективно, пероксильные радикалы устраняют витамин А. (16) Существуют доказательства того, что витамин К, который обычно не считается антиоксидантом, может ингибировать перекисное окисление липидов. (17) Некоторые важные диетические минералы, хотя и не действуют как прямые поглотители радикалов, однако являются неотъемлемой частью антиоксидантных ферментов (металлоферментов), например, селен-глутатионпероксидаза и тиоредоксинредуктаза, железная каталаза, цинк и медь-цитозольный супероксид дисмутаза — митохондриальная.
Помимо того, что растительная пища богата витаминами и минералами-антиоксидантами, она также содержит множество фитохимических веществ, полезных для здоровья человека. К ним относятся фенольные кислоты, флавоноиды, каротиноиды, фитостерины и растительные волокна. Эти фитохимические вещества являются предметом обширных исследований, посвященных их участию в различных процессах, в которых они могут играть разные роли, такие как антиоксидантные, противовоспалительные, сосудорасширяющие и антипролиферативные. Среди биологических функций, упомянутых выше, наиболее часто изучается антиоксидантная активность, поскольку она способствует укреплению здоровья и предотвращению заболеваний человека.
Каротиноиды — это группа липофильных пигментов, которые синтезируются растениями и придают ряду фруктов и овощей яркий цвет. Наиболее распространенными каротиноидами являются ликопин, α- и β-каротин, зеаксантин и лютеин. Основной антиоксидантный эффект каротиноидов объясняется их участием в угасании синглетного кислорода. (18) После завершения реакции гашения возбужденные каротиноиды высвобождают вновь приобретенную энергию посредством серии вращательных и колебательных взаимодействий с растворителем, а затем возвращаются в невозбужденное состояние. Антиоксидантная активность каротиноидов была идентифицирована и наблюдалась в лаборатории, однако в естественных условиях их антиоксидантное действие на организм человека еще не было надежно протестировано. (18) Полифенолы — фенольные кислоты, флавоноиды, дубильные вещества и лигнаны — обладают мощными антиоксидантными свойствами при введении в дозах, превышающих те, которые обычно употребляются людьми с пищей или диетическими добавками. Этот вывод подтверждается лабораторными экспериментами на животных. Полифенолы способны ингибировать широкий спектр активных форм окислителей, включая O2–, OH, HOCl, пероксинитриты и пероксильные радикалы. (19, 20) Кроме того, они хелатируют ионы переходных металлов (железо и медь), чтобы предотвратить образование радикалов, индуцированных переходными металлами. (21)
Общая антиоксидантная защита организма, включая эндогенную и экзогенную подсистемы, функционирует как единая связная система с целью устранения реактивных типов оксидантов. Однако некоторые окислители все же не защищаются и вызывают окислительное повреждение организма. В антиоксидантных ферментах супероксиддисмутаза превращает O2 в H2O2, затем H2O2 восстанавливается до H2O (вода). В этом случае медиаторами выступают каталаза или глутатионпероксидаза. Для низкомолекулярных антиоксидантов витамин E ослабляет свободные радикалы и, таким образом, сам становится слабым свободным радикалом. Впоследствии радикалы витамина E обрабатываются или восстанавливаются до своей исходной формы с помощью витамина C, липоловой кислоты или кофермента Q10. (1, 3) Радикалы витамина С могут быть дополнительно восстановлены с помощью глутатиона, а окисленная форма восстанавливается с помощью глутатионредуктазы за счет пентозофосфатного пути НАДФН, а в качестве субстрата используется глюкоза. Полифенолы зарекомендовали себя в экспериментальных лабораторных условиях как мощный антиоксидант, устраняющий радикалы. Однако в естественных условиях действие полифенолов как антиоксидантов довольно ограничено, в основном из-за их низких концентраций в кровотоке и тканях (<1 мкмоль / л, что намного ниже содержания витаминов C и E), а также из-за их экстенсивного превращения в форму, в которой они теряют свою антиоксидантную способность. (22) Вопреки преобладающей идее о том, что полифенолы сами по себе являются сильным антиоксидантом, устраняющим радикалы, они способствуют антиоксидантной защите только за счет усиления регуляции эндогенной антиоксидантной системы, например, за счет увеличения производства глутатиона и повышения активности глутатионпероксидазы. (23)
Хотя механизм, который мог бы точно объяснить регулирующее и улучшающее действие полифенолов, до конца не изучен, все еще утверждается, что индукция вызвана их слабым окислительным действием во время быстрого окисления с образованием H2O2 и других продуктов окисления. (3) Однако антиоксидантный эффект полифенолов in vivo находится под тщательным контролем. Обсуждаемые здесь потенциальные преимущества для здоровья возникают в желудочно-кишечном тракте, когда полифенолы присутствуют в своей первоначальной форме в высоких концентрациях. (24)
Универсальные патогенетические механизмы патологических состояний:
1. Чрезмерное и неконтролируемое улучшение эндогенной антиоксидантной системы (АОС) процессов ПОЛ.
2. ГИПОКСИЯ — недостаточное снабжение или потребление кислорода клетками и тканями организма. При этом гипоксия и перекисное окисление липидов взаимно усиливают друг друга, что приводит к нарушению энергетических и обменных процессов в клетках и тканях (рис. 3).
Причины начать (усилить) секс:
- Стресс (любого происхождения);
- Ишемия;
- Гипоксия;
- Реперфузия тканей (реперфузионный синдром);
- Воспаление (асептическое или бактериальное);
- Недостаточная активность физиологической антиоксидантной системы (относительная или абсолютная).
Фотоизображение клеток при помощи конфокального микроскопа

Здоровые клетки Белковые агрегаты, образующиеся в клетках
в окислительном процессе
Рис. 1. Патологическая роль оксидативного стресса
Причина развития оксидативного стресса (ОС) — накопление в организме лишних свободных радикалов. Короткоживущие нестабильные радикалы — это небольшие молекулы гидроксильного радикала ОН 02- и большие молекулы радикала, несущие так называемый центрированный радикал, в котором неспаренный электрон находится около любого атома этой молекулы (радикалы с центром на углероде R-CH2-CH — CH2 . или центрированные углеродно-кислородные радикалы R-00) кислород. Долговечные стабильные радикалы, когда неспаренный электрон делокализован между многими атомами (радикал аскорбата, радикалы кофермента Q, радикал токоферокси).
Стабильность центрированного радикала зависит от положения окружающих химических групп в молекуле. Например, некоторые нитроксильные радикалы, хотя и не имеют электрона, делокализованного по атому кислорода, стабильны благодаря наличию групп CH3, которые «защищают» радикальный центр от контакта с другими молекулами.
При столкновении с молекулой свободный радикал отрывает атом водорода (рис. 2). Образуется насыщенная валентностью молекула, которая превращается в свободный радикал. Он может оторвать атом водорода от другой молекулы или вступить в реакцию с другим радикалом или молекулой кислорода. Пероксидный радикал ROO извлекает атом водорода из другой молекулы, и образуется органический пероксид ROOH. Эта вырожденная цепная реакция называется ПРОЦЕССОМ САМОКИСЛИВАНИЯ УГЛЕВОДОРОДОВ ИЛИ СВОБОДНЫМ РАДИКАЛЬНЫМ ОКИСЛЕНИЕМ (FRO).

Рис. 2. Окисление свободных радикалов
Основные механизмы патологии при любом критическом состоянии — это процессы свободных радикалов и изменение свойств клеточных биомембран. При ишемии тканей, особенно в головном мозге и миокарде, основная патологическая роль свободных радикалов заключается в том, что они активно взаимодействуют с молекулами, образующими нейрональные и внутриклеточные мембраны. Увеличивается вязкость мембран, теряется их пластичность и функциональное состояние.
Определенную опасность представляет восстановление кровотока в ранее ишемизированных тканях. Реперфузия вызывает многократное повышение парциального давления кислорода с дальнейшим усилением радикальных процессов. В этом случае повреждается эндотелий капилляров, антикоагулянтная активность которых трансформируется в прокоагулянт.
Лейкоциты и тромбоциты из-за увеличения адгезии закупоривают капилляры головного мозга. Этот процесс усугубляется увеличением жесткости эритроцитов, что значительно усиливает нарушение оксигенации тканей, особенно головного мозга. Угнетаются процессы фибринолиза крови, увеличивается область поражения тканей, инфаркт мозга, увеличивается отек мозга. Существует прямая зависимость между накоплением продуктов ПОЛ и тяжестью поражения мозга и других тканей. Наряду с этим активируются гены, ответственные за запрограммированную гибель клеток — апоптоз.
Инструментарий для оценки окислительного стресса
Окислительный стресс можно рассматривать как следствие борьбы между антиоксидантной защитой и реактивными типами оксидантов. Некоторые из наиболее реактивных типов окислителей способны уклоняться от защиты и вызывать окисление чувствительных макромолекул (липидов, ДНК и белков). Количество образующихся продуктов окисления зависит от соотношения между антиоксидантной защитной способностью организма и количеством и реакционной способностью активных форм окислителя. Теоретически состояние окислительного стресса в организме может быть лучше выяснено, если оценить элемент системы антиоксидантной защиты и реактивные типы оксидантов и окисленных продуктов. Однако практически невозможно измерить высокореактивные типы оксидантов в организме человека, поскольку они удерживаются в нем в течение секунды (или даже меньше) после их образования. Количественная оценка низкомолекулярных антиоксидантов и измерение активности антиоксидантных ферментов могут быть выполнены достаточно качественно. В этом случае процесс измерения может быть довольно громоздким, так как действие каждого фермента необходимо оценивать индивидуально. Таким образом, одним из лучших биологических маркеров для оценки состояния окислительного стресса в организме человека являются продукты, полученные из реактивных типов оксидантов.
Надежные биологические маркеры способны адекватно отражать состояние соответствующих физиологических функций организма, обнаруживать наличие признаков патологий, а также устанавливать, оказывает ли тот или иной агент положительное, отрицательное или не влияет на улучшение здоровья человека, или служит для целей профилактики заболеваний, или имеет терапевтическое значение при лечении существующих заболеваний. Когда реактивные окислители атакуют нуклеофилы с целью захвата электронов, следствием этих атак является производство различных продуктов окисления. Анализы для определения продуктов окисления липидов, белков и ДНК были рассмотрены в другом месте. (25, 26) Короче говоря, малоновый диальдегид (MDA) и F2a-изопростаны (iPF2) являются двумя распространенными биомаркерами перекисного окисления липидов, причем последний более чувствителен и специфичен. MDA, как правило, исследуется чаще, чем iPF2. Это связано с относительно невысокой стоимостью исследования и высоким выходом МДА в различных матрицах. Однако надежность результатов таких исследований и их специфичность часто ставятся под сомнение из-за перекрестного взаимодействия 2-тиобарбитуровой кислоты (образующей розовый аддукт с МДА) с другими субстратами (другими алканами, белками, сахарозой, аминокислотами, сиаловой кислотой) кислота, мочевина, ацетальдегид-сахароза и редуцирующие сахара). Белки могут быть повреждены непосредственно атакой свободных радикалов или косвенно = через реакцию с участием вторичных побочных продуктов перекисного окисления липидов. В результате этого типа реакций образуются окислительно модифицированные аминокислоты и карбонильные белки (БА) соответственно. (27) Последние являются наиболее часто используемыми биологическими маркерами окисления белков в исследованиях на людях. Этот маркер можно измерить колориметрическим анализом, иммуноферментным анализом (ELISA) или методом ВЭЖХ. (28, 29) Окисленные аминокислотные продукты, такие как хлортирозин (Cl-tyr), 3-нитротирозин (N-tyr) и дитирозин (di-tyr), более указывают на специфические радикальные реакции с белками, чем карбонилы белков. (30) В частности, продукты окисления тирозина образуются исключительно в естественных условиях и не подвержены артефактам. (29) Были разработаны методы с использованием ВЭЖХ с электрохимическим детектором (ECD) или ГХ-МС для количественного определения окисленных аминокислот. Основания окисленной ДНК, которые отражают повреждение ДНК и указывают на риск развития рака, могут быть изучены и оценены с использованием различных методов, например HPLC-ECD, GC-MS, LCD-MS и ELISA. Кроме того, индуцированные радикалами разрывы цепи ДНК можно частично определить в отдельных клетках с помощью электрофореза одной клетки. Этот метод еще называют «кометным» анализом. (31) Из окисленных оснований ДНК наиболее часто измеряется 8-гидроксигуанониз (8-оксо-DH).
Анализ отдельных низкомолекулярных антиоксидантов занимает много времени и обычно требует хроматографического разделения перед количественным определением. Следовательно, количественное определение всех возможных антиоксидантов в продуктах питания и жидкостях человека — очень трудоемкий и дорогостоящий процесс. Кроме того, некоторые фитохимические антиоксиданты, содержащиеся в пище, еще предстоит охарактеризовать. С учетом всего вышеперечисленного ученые на протяжении многих лет разработали множество простых в использовании и недорогих методов, чтобы предоставить общий метод измерения антиоксидантной способности всех антиоксидантов, содержащихся в пище или плазме / сыворотке. Сюда входят измерения антиоксидантных свойств, таких как их способность устранять кислородные радикалы, антиоксидантная способность восстанавливать железо, способность ингибировать дифенилпикрилгидразил, антиоксидантная способность, эквивалентная тролоксу, и общая способность удалять радикалы в целом. (32) Такие исследования необходимы для выявления связи между потреблением продуктов, богатых антиоксидантами, и риском развития определенных заболеваний, а также для оценки влияния различных питательных веществ, продуктов или диет на антиоксидантный статус человека. Среди процитированных выше исследований наиболее признанным является изучение способности антиоксидантов устранять кислородные радикалы, поскольку результаты этого конкретного анализа часто используются пищевыми компаниями для продвижения своей продукции на потребительском рынке. Использование всех этих типов анализа в исследованиях пищевых продуктов остается привлекательным для профессионалов в области пищевых продуктов, поскольку они помогают определить истинную ценность пищи. Однако есть опасения, что антиоксидантные свойства пищевых веществ могут не быть напрямую связаны с антиоксидантами в плазме / сыворотке, поскольку диетические антиоксиданты претерпевают значительные изменения во время жевания, в желудочно-кишечном тракте при воздействии желудочного сока и метаболических процессов кишечных бактерий. И эндогенного происхождения механизмы детоксикации.
Связь, которая существует между накоплением биологических маркеров окислительного повреждения и производством определенного свободного радикала, является лишь косвенной, поскольку изменение клиренса может резко изменить уровень маркера без изменения продукции данного свободного радикала. Поэтому анализ характеристик продуктов, приводящих к окислительному повреждению, следует проводить с осторожностью, четко понимая, что именно поможет идентифицировать используемые методы. Также важно понимать, что антиоксидантная способность in vivo определяется не только реактивностью по отношению к радикалам, но и рядом других факторов, таких как концентрация, распределение, расположение, судьба антиоксидантного радикала, его взаимодействие с другими антиоксидантами и метаболизм. Невозможно надежно оценить общий окислительный стресс, как локально, так и системно, с использованием одного биологического маркера. Биомаркеры следует выбирать, исходя из того, какие функции и индикаторы будут оцениваться. Более того, комбинированная оценка как биологических маркеров «следа» реактивных оксидантов, так и антиоксидантной защиты организма, включая ферментативные и неферментативные формы защиты, — лучший способ определить роль свободных радикалов и организмов в биологии и медицине.
- http://www.sibmedport.ru/article/8373-okislitelniy-stress-globalnaja-problema-meditsini-kriticheskih-sostojaniy-chast-1/
- https://FoodandHealth.ru/komponenty-pitaniya/antioksidanty/
- https://www.ProPlan.ru/vet/zdorove/article/poleznost-pischevykh-antioksidantov-dlya-zdorovya-protivorechiya-i-proverka